2023年8月10日,我院林世贤课题组在Nature Chemical Biology (自然化学生物学)杂志发表了题为“Computational design and genetic incorporation of lipidation mimics in living cells”的研究论文。该研究开发了计算机辅助的筛选策略,设计了系列完全模拟天然脂化修饰的非天然氨基酸,并实现了脂化修饰的遗传编码。论文进一步利用脂化修饰的遗传编码系统研究了多种蛋白质脂化修饰的生物学功能,测定了蛋白质结合细胞膜的能力,探索了脂化修饰蛋白膜定位的碳链长度规律,并构建和评价了半衰期延长的、遗传编码的脂化蛋白质药物。
在所有与膜相关的生物学过程中, 蛋白质脂化修饰(lipidation)几乎都发挥着重要作用。蛋白质翻译中或翻译后,脂化修饰通过将强疏水性的脂质分子共价连接到蛋白质的特定位点上,从而重塑蛋白质与膜,蛋白质与蛋白质的相互作用。虽然细胞中有上千种蛋白质存在脂化修饰,但由于脂化修饰存在着高度可变、可逆以及与其它翻译后修饰串扰等特点,大多数蛋白质上的脂化修饰的功能仍不明确。同时,脂化修饰的多肽或蛋白质药物通过结合血清白蛋白,显著延长了药物的血清半衰期。因此,脂化修饰是经临床证实的长效药物的重要开发策略,被成功地应用于多个重磅的上市药物中。然而,适用于哺乳动物细胞体系的、模拟天然脂化修饰的位点特异性脂化修饰策略仍然缺失,限制了蛋白质脂化修饰的功能解码以及精准脂化修饰药物的研发。
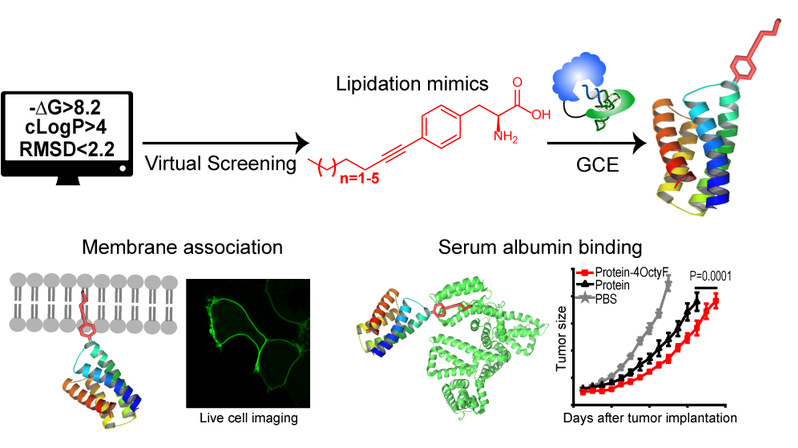
图1、遗传编码脂化修饰系统的计算机辅助开发及其生物医药应用。
林世贤课题组首先开发了一种计算辅助的评价策略,虚拟评估了数百种脂化修饰非天然氨基酸的疏水性,白蛋白结合力,及其被正交翻译系统识别的可能性。计算机辅助的评估发现了一类含有芳香环和线性脂肪族侧链的非天然氨基酸能够完全模拟天然脂化修饰的膜定位和白蛋白结合的生化特性。同时,利用其课题组开发和优化的嵌合体翻译系统,实现了多个长度可调的脂化修饰的遗传编码,并在多种功能蛋白质上高效、特异地引入脂化修饰。进一步的生化实验表明,多种遗传编码的脂化修饰蛋白质与天然脂化修饰蛋白质具有相同的细胞膜结合能力和生物学功能。通过遗传编码不同长度的脂化修饰,研究发现脂化修饰的疏水性强弱是决定其能否具有稳定质膜结合的重要参数,且具有13个碳和15个碳长度的脂肪链具有截然不同的细胞质膜锚定特性。这一发现很好地解释了哺乳动物细胞中大多数蛋白质的脂化修饰碳链长度最少是14个。最后,通过将脂化修饰精准地展示在药物蛋白质上,能够将药物蛋白结合血清白蛋白的亲和力提升至nM水平,从而显著延长药物蛋白的血清半衰期,在小鼠肿瘤模型中展示出了更好的抗肿瘤能力。
我院博士后丁文龙和博士生刘超是论文的共同第一作者,林世贤研究员是本文的通讯作者。研究工作得到了冯新华教授、何向伟教授、袁瑛教授、张龙教授,以及生命科学研究院共享技术平台的大力支持与帮助。该研究受国家重点研发计划“合成生物学”项目,国家重大研究计划“生物大分子动态修饰与化学干预”项目等项目的资助。
原文链接:https://www.nature.com/articles/s41589-023-01400-8
林世贤实验室聚焦于中心法则的翻译过程,整合交叉学科的研究手段,探索tRNA和蛋白质修饰的生物学功能和工程改造,并致力于开发新型生物医药,用于重大疾病和罕见遗传病的诊疗。欢迎感兴趣的博士后和研究生联系并申请加入。实验室链接:/25713/list.htm




