2023年7月11日,我院林世贤实验室在美国化学会志(Journal of the American Chemical Society)上在线发表题为“Manipulating cation-π interactions of reader proteins in living cells with genetic code expansion” 的研究论文。该论文报道了一种工程改造活细胞内阳离子-π相互作用的广谱型策略,通过构建系列组蛋白甲基化修饰的超级读码器,在活细胞中实现对组蛋白甲基化修饰的富集、原位检测和微环境分析。这一研究是其实验室开发的嵌合体翻译系统的一项重要延伸应用,为活细胞中组蛋白甲基化修饰的精准调控与交互作用网络研究提供了化学生物学策略。据悉,该论文还将入选JACS杂志的封面文章。我院博士后赵红霞,博士生唐玲、方誉是论文的共同第一作者,林世贤研究员是本文的通讯作者。
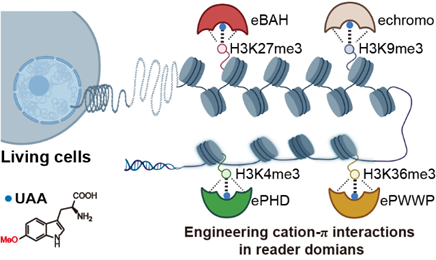
图1. 活细胞内工程改造组蛋白甲基化读码器增强阳离子-π相互作用的示意图。
阳离子-π相互作用是发生在阳离子与共轭π电子云之间的一种非共价相互作用,其在生物分子的自组装、分子识别、分子黏连和分子折叠中扮演重要作用,特别是在神经递质受体-配体识别和组蛋白甲基化解码等重要生物过程中发挥着核心功能。尽管在理解阳离子-π相互作用的机理和生物功能方面取得了巨大的成功,但在活细胞中设计和合成增强的阳离子-π相互作用的研究基本空白。
2022年,利用其实验室开发的嵌合体翻译系统,林世贤实验室报道了一种利用遗传密码扩展技术将组蛋白甲基化修饰读码器的“芳香笼”结构中高度保守的氨基酸替换为强给电子基团取代的芳香族氨基酸,显著提升其介导的阳离子-π相互作用的策略1。然而,该方法仅限于体外应用,其在活细胞中的适用性仍未可知,活细胞内原位调控阳离子-π相互作用的工具亟待开发。
基于此,林世贤实验室首先设计并合成了几种富含给电子取代基的色氨酸衍生物:6, 7-甲基-色氨酸(DiMeW)、6, 7-甲氧基-色氨酸(DiMeOW)和6,7-二氢呋喃-色氨酸(DHFW),并利用遗传密码扩展技术成功地将其引入到组蛋白甲基化读码器中,以操纵各种读码器的阳离子-π相互作用。与上述色氨酸衍生物相比,他们发现使用6-甲氧基-色氨酸(6MeOW)取代读码器芳香笼中的关键色氨酸能最大程度提升其阳离子-π相互作用的结合能。研究证明该策略广泛适用于设计系列组蛋白H3甲基化结合亲和力增强的读码器,包括H3K4me3、H3K9me3、H3K27me3和H3K36me3的读码器。相比于低亲和力的天然读码器,工程改造的超级读码器可实现活细胞内组蛋白甲基化的富集与成像,具有更高的信噪比;此外,他们结合邻近标记技术,利用工程改造的超级读码器有效捕获了活细胞中组蛋白修饰微环境中的蛋白质组,为组蛋白修饰的原位检测与调控提供了新的研究思路。
该工作得到了国家重点研发计划“合成生物学”,国家重大研究计划“生物大分子动态修饰与化学干预”,国家自然科学基金和中国博士后科学基金等项目资助,以及生命科学研究院共享技术平台的马杰、蒋雪樱、张夏俊等人的大力支持与帮助。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.3c02293
Reference:
1.Zhao, H.; Liu, C.; Ding, W.; Tang, L.; Fang, Y.; Chen, Y.; Hu, L.; Yuan, Y.; Fang, D.; Lin, S., Manipulating Cation-π Interactions with Genetically Encoded Tryptophan Derivatives. Journal of the American Chemical Society 2022, 144 (15), 6742-6748.





