卵母细胞是动物体内最大的细胞,在她的生长过程中,细胞质中储存了大量母源性mRNA,但是这些mRNA处于翻译抑制状态,而且保持稳定,不被降解。当卵母细胞生长到足够大小以后,自身的转录活动就终止了。随后的两次减数分裂和受精过程完全受到卵胞质中母源性mRNA和蛋白质的调控。生长中的卵母细胞其细胞周期阻滞在第一次减数分裂前期,直到排卵前几个小时才恢复减数分裂。同时,卵胞质中贮存的mRNA开始被活跃翻译成蛋白质。这些新合成的蛋白质对于减数分裂细胞周期进程、纺锤体组装、染色体分离都具有重要的调控作用。并且,这些母源性mRNA在完成蛋白翻译功能之后被迅速降解。但是,卵母细胞中母源性mRNA的翻译和降解是如何调控的呢?这在以前并不十分清楚。
范衡宇实验室研究发现,是MAPK信号级联通路把母源性mRNA的翻译和降解是如何与卵母细胞减数分裂进程偶联在一起。十几年前人们就发现,该信号通路在卵母细胞恢复减数分裂以后被激活,并且在卵母细胞成熟过程中具有重要生理功能,但是一直未能阐明其关键作用机制。范衡宇课题组发现,MAPK信号通路的关键蛋白激酶ERK1/2直接磷酸化激活细胞质中的RNA结合蛋白CPEB1,后者激活以后,通过结合mRNA 3’不翻译区(3’-URT)的CPE位点,促进mRNA 3’-poly(A)尾的延长并启动蛋白翻译。受这一机制调控的重要母源性mRNA包括编码纺锤体组装的Dazl和Tpx2、以及调控细胞周期进程的Cyclin B。并且,ERK1/2和CPEB1诱导BTG4和CNOT7蛋白翻译,从而以负反馈形式启动了母源性mRNA降解过程。范衡宇实验室在国际上首次构建了卵母细胞特异性ERK1/2基因敲除小鼠模型,通过表型分析,发现缺失ERK1/2的卵母细胞具有严重的纺锤体组装和减数分裂缺陷,并且受精之后不能启动早期胚胎发育进程,从而用体内实验模型进一步验证了上述生化过程的生理意义。
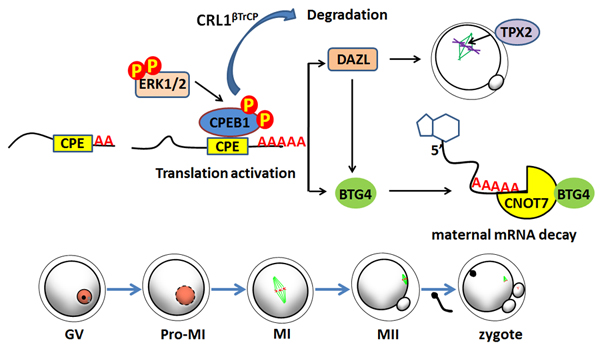
ERK1/2在卵母细胞成熟过程中启动母源性mRNA翻译的分子机制示意图
这项研究近日在线发表在国际发育生物学知名期刊Development上,题为“MAPK Cascade Couples Maternal mRNA Translation and Degradation to Meiotic Cell Cycle Progression in Mouse Oocyte”。
全文请见:http://dev.biologists.org/content/early/2016/12/17/dev.144410




